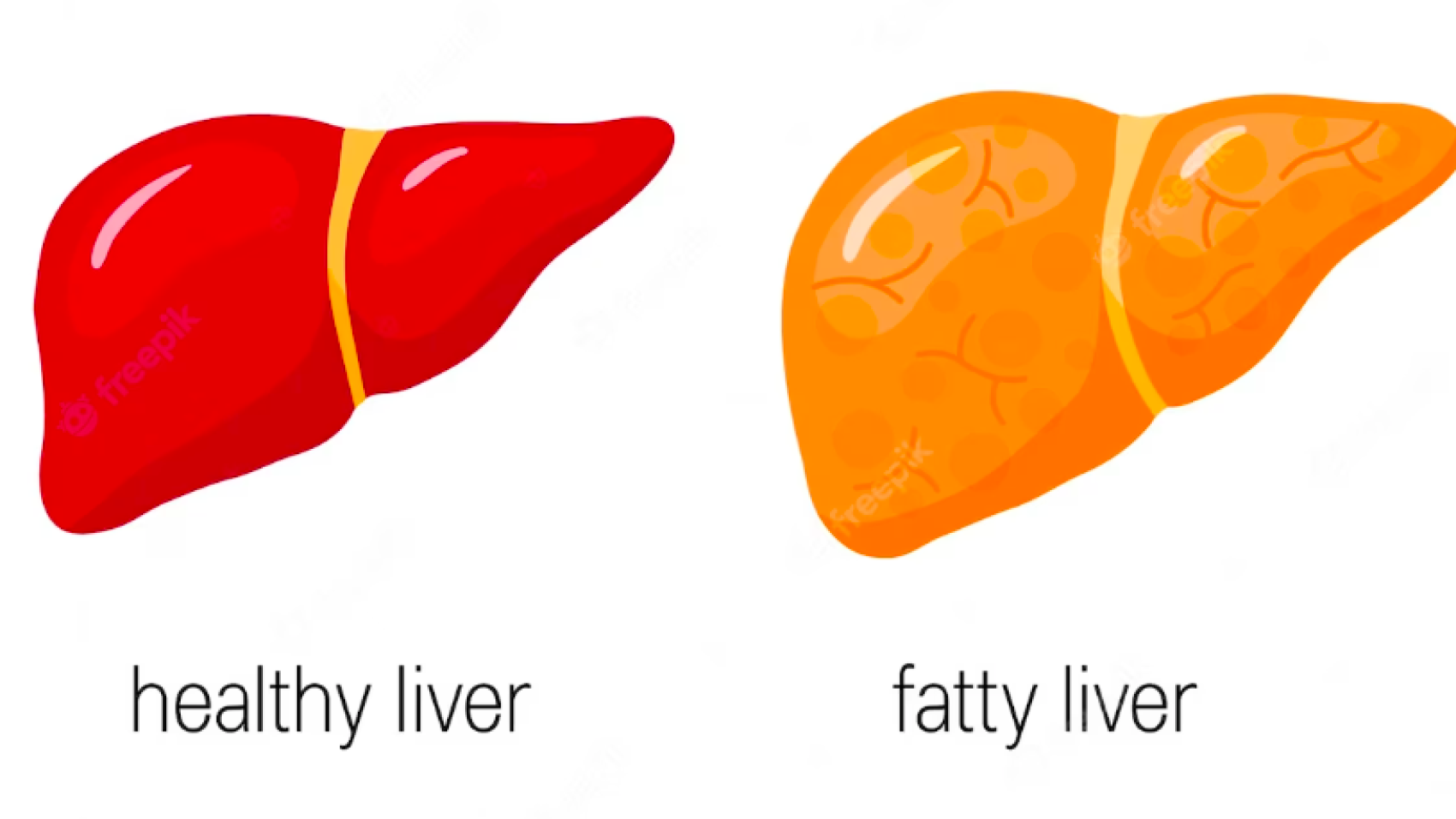
Исследователи из Cedars-Sinai Cancer обнаружили, что ожирение печени, состояние, тесно связанное с ожирением, способствует распространению колоректального рака на печень.
Экихиро Секи(автор исследования) отметил, что в исследовании изучалась легкая форма жировой дистрофии печени, о которой клиницисты могут не знать или не искать. Он также подчеркнул, что это состояние, вероятно, недооценивается.
«Наше исследование показало, что даже легкая степень ожирения печени увеличивает риск распространения рака», — сказал Секи. «Таким образом, мы призываем врачей действительно обратить внимание на пациентов с колоректальным раком, у которых может быть жировая дистрофия печени. Среди наших выборок пациентов мы отметили, что более 40% пациентов имели жировую дистрофию печени, но врачи часто не назначают специализированную МРТ, необходимую для обнаружить его, а это означает, что многие случаи упущены».
По словам Секи, в конечном итоге у 70% пациентов с колоректальным раком разовьются метастазы в печень, что является основной причиной смерти этих пациентов. Он и его коллеги-исследователи стремились выяснить, почему у одних пациентов развиваются агрессивные метастазы, а у других нет, и определить, почему только некоторые пациенты хорошо реагируют на терапию.
«Наша гипотеза заключалась в том, что ожирение печени как-то влияет на эти различия», — сказал Секи.
Секи и его команда исследовали лабораторных мышей с метастазами колоректального рака в печень, некоторые из которых получали диету с высоким содержанием жиров, из-за чего у них развилась жировая печень. Они отметили, что клетки печени у мышей с ожирением печени продуцируют большее количество внеклеточных везикул — частиц, которые высвобождаются из клеток и несут белки и генетический материал из родительской клетки.
«Внеклеточные везикулы, продуцируемые жировыми клетками печени, содержат три типа микроРНК, которые стимулируют пролиферацию, миграцию и инвазию рака», — сказал Секи. «Раковые клетки захватывают эти внеклеточные везикулы, и эти микроРНК реагируют с другим белком, называемым yes-ассоциированным белком, чтобы способствовать росту опухоли. Таким образом, первичный рак у мышей с ожирением печени становится более агрессивным и более метастатическим».
Исследователи обнаружили те же типы состояний, когда сравнивали образцы тканей пациентов с ожирением печени и без него, у которых также были метастазы колоректального рака в печень.
«Это исследование дает новое представление о механизмах, лежащих в основе жировой дистрофии печени, способствующей метастазированию колоректального рака, а также о различных микроокружениях опухоли у пациентов с жировой дистрофией печени, которые могут способствовать слабому ответу на противораковую терапию», — сказал Дэн Теодореску, доктор медицинских наук. директор Cedars-Sinai Cancer и почетный председатель PHASE ONE. «У нас есть постоянные усилия, направленные на группы населения с высоким риском жировой болезни печени, и это исследование предполагает, что нам необходимо удвоить наши усилия, особенно в отношении тех, у кого есть колоректальный рак».